Кріопреципітат заморожений
Назва: “Кріопреципітат заморожений”
Основні властивості:
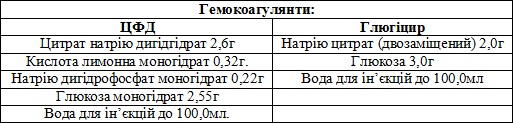
Кріопреципітат заморожений – білковий компонент плазми крові людини, що містить не менше 70 МО фактору VIII (антигемофільного глобуліну-АГГ) в одній дозі- та не менше 140 МО в двох дозах, являє собою осад кріоглобулінів білого кольору з 30–40 мл або з 65 -75 мл залишкової плазми у замороженому стані,і отриманий з однієї чи двох доз свіжозамороженої плазми об’ємом відповідно не менше 200,0 або 400,0 мл. У замороженому стані – тверда маса жовтуватого кольору, а при розморожуванні і розчиненні на водяній бані при температурі від 35-37оС – прозора жовтуватого кольору рідина, не містить механічних домішок, пластівців. Компонент донорської крові, заготовленої на гемокоагулянтах ЦФД та Глюгіцир, виготовлений з карантинизованої плазми, стерильний ,тестований на антитіла до ВІЛ-1/2, вірусу гепатиту С, збудника сифілісу, поверхневий антиген вірусу гепатиту В.
Фармокологічні властивості – кріопреципітат виявляє антигеморагічну дію при підвищених кровотечах, пов’ язаних із зниженням активності і вмісту антигемофільного глобуліну (ф.VIIIc), фактору Віллебранта (ф.VIIIvW), фібринстабілізуючого фактору(ф.XIII) та фібриногену (ф.І).
Лікарська форма: розчин
Показання до застосування:
Кріопреципітат призначається для лікування та профілактики кровотеч у хворих на гемофілію А, хворобу Віллебранта (ангіогемофілія), гіпо- та афібріногенемії, при гострій масивній крововтраті із різким зниженням факторів згортання крові та при синдромі дисемінованого внутрішньосудинного згортання.
Спосіб застосування:
Кріоприципітат заморожений застосовують з урахуванням груп крові за системою АВО. Безпосередньо перед використанням кріопреципітат розморожують протягом 6-8 хвилин на водяній бані при температурі від 35оС до 37оС, обережно перемішують вміст контейнерів похитуючими рухами до повного розчинення осаду кріоглобулінів у плазмі. Під час розморожування та розчинення компоненту не допускати різких поривчастих рухів з метою збереження антигемофільного глобуліну.
Після проведення макроскопічної оцінки та перевірки на герметичність компонент крові відразу переливають пацієнту. Вводять кріопреципітат внутрішньовенно струминно повільно, за допомогою систем для переливання крові одноразового застосування с діаметром пор фільтру не більше 170-200 мкм. Розморожений кріопреципітат не підлягає повторному заморожуванню!
Основна мета гемостатичної терапії кріопреципітатом полягає в підвищенні вмісту дефіцитного фактору VIII в крові хворого до ефективного рівня.
Для забезпечення ефективного гемостазу при найбільш частих ускладненнях гемофілії (гемартрози, ниркові, ясневі та носові кровотечі) вміст фактору VIII в плазмі крові хворого необхідно підтримувати на рівні не нижче 20%. Для цього вводять кріопреципітат в добовій дозі 15-20 МО/кг.
При міжм’язових гематомах, шлунково-кишкових кровотечах, переломах кісток, травмах та при видаленні декількох зубів – не нижче 30%. Для цього вводять кріопреципітат у добовій дозі 35 – 40 МО/кг.
У випадку профузних шлунково-кишкових кровотеч, значних травм, макрогематурії, заочеревинних гематомах, гематомах, які тиснуть на дихальні шляхи, крововиливах у центральну нервову систему необхідна концентрація фактору VIII в крові хворого не менше 50%. Для цього вводять кріопреципітат в добовій дозі 50 – 70 МО/кг.
Після повної зупинки кровотечі введення підтримуючих доз кріопреципітату хворим на гемофілію здійснюють з інтервалом 12 – 24 години та у дозі, яка забезпечує підтримку вмісту фактору VIII на рівні не нижче 15% (10–20 МО/кг) протягом декількох діб до зняття запальних змін або зменшення розмірів гематоми.
При більшості хірургічних втручань необхідно підтримання вмісту антигемофільного глобуліну в крові хворого на рівні не нижче 50% під час операції та 30% в післяопераційному періоді. Для цього за 30 хв до операції одномоментно вводять гемостатичну дозу кріопреципітату з розрахунку 45-60МО/кг, через 8-12 годин дозу повторюють. В післяопераційному періоді вводять компонент в добовій дозі 20-30МО/кг через кожні 12- 24 години на протязі 3-5 діб, а в подальшому-10-20МО/кг. При масивній кровотечі під час хірургічного втручання виконують заміщення крововтрати та введення кріопреципітату в кінці операції в дозі, рівній половині первинної.
Побічна дія:
Під час введення кріопреципітату у деяких пацієнтів можуть відмічатися парестезія ротової порожнини, яка проходить по закінченні трансфузії і не потребує лікування. У пацієнтів сенсибілізованих до антигенів формених елементів крові і плазми, введення кріопреципітату може викликати незначний озноб та підвищення температури. Реакція корегується застосуванням антигістамінних засобів.
Протипоказання:
Абсолютних протипоказань для переливання компоненту немає.
Умови зберігання і термін придатності:
Зберігати в морозильній камері при температурі не вище мінус 20°С. Температурний режим зберігання передбачає проведення цілодобового моніторингу. Термін придатності: до 12 місяців з моменту заготівлі плазми свіжозамороженої.
Транспортування:
Для гарантованого збереження повноцінності компонету система транспортування має забезпечити температуру не вище мінус 20° С в кінці терміну транспортування. Транспортні засоби без рефрижератора повинні буди обладнані термоізолюючим контейнером з акумулятором холоду, охолодженим до температури нижче мінус 30° С.
Лікувальний заклад при отриманні компоненту повинен впевнитись, що кріопреципітат залишався в замороженому стані на протязі всього періоду транспортування. При відсутності термінового переливання його необхідно відразу помістити на зберігання при рекомендованих температурних умовах для подальшого зберігання.
Пакування: в полімерних контейнерах по 35,0±5 мл або 70,0±5 мл.
Виробник: КНП ХОР “Обласний центр служби крові”, Україна.
Адреса:61051, м. Харків, вул. Клочківська, 366, тел. (057) 341-48-78
e-mail: KHOCSK@ukr.net
Експедиція КНП ХОР “Обласний центр служби крові” працює цілодобово: тел. (057) 341-48-78
Нормативні посилання:
1. Наказ МОЗ України №211 від 09.03.2010 “Порядок контролю за дотриманням показників безпеки та якості донорської крові та її компонентів”.
2. Наказ МОЗ України № 385 від 01.08.05р. «Про інфекційну безпеку донорської крові та її компонентів».
3. Методичні рекомендації «Заготівля та використання кріопреципітату замороженого», Київ-2006.
