Відмиті еритроцити
Назва: “Відмиті еритроцити”
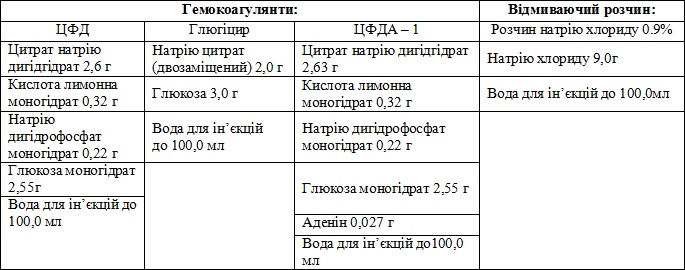
Основні властивості – еритроцити з видаленням залишків плазми, антикоагулянту, електролітів, лейкоцитів і тромбоцитів шляхом використання відмиваючих розчинів, мануальним або апаратним методом, що зменшує реактивність цього середовища.
Склад: об’єм однієї дози складає (200±20) мл; вміст гемоглобіну не менше 40 г/дозу, гемоліз – менше 0,8% маси еритроцитів наприкінці терміну зберігання, лейкоцитів менше 1,0×106 в дозі, білку менше 0,5% г/дозу.
Лікарська форма: розчин.
Показання: відновлення втрати крові та лікування анемій у пацієнтів з антитілами білків плазми, особливо анти-IgA, а також у пацієнтів, які мали серйозні алергічні реакції під час трансфузій продуктів крові.
Спосіб застосування і дози:
«Еритроцити відмиті» вводять внутрішньовенно крапельно зі швидкістю, що не перевищує 40-60 крапель на хвилину, а при шокових станах – внутрішньоартеріально. Дозу встановлюють індивідуально. Разова доза залежить від стану пацієнта, може обмежуватись однією дозою, а при необхідності 2-3 дозами. У похилому віці слід уникати надмірної кількості використання компоненту і швидкого його введення, оскільки це може привести до перевантаження серцево-судинної системи. Для зменшення густини еритроцитів хворим з реологічними і мікроциркуляторними порушеннями безпосередньо перед трансфузією в кожну дозу слід додавати 50,0-100,0мл стерильного 0,9% розчину натрію хлориду.
Побічна дія: перевантаження системи кровообігу; гемолітичні реакції трансфузій; сепсис через ненавмисне бактеріальне забруднення крові; передача вірусних агентів (ВІЛ 1/2, гепатитів), сифілісу, можливе навіть за умови ретельного відбору донорів і використання процедур скринінгу; аллоімунізація проти НLА-антигенів і антигенів еритроцитів; передача інших патогенів, присутність яких не перевірялась за допомогою тестів або вони не були розпізнані.
Протипоказання:
Абсолютних протипоказань для переливання відмитих еритроцитів немає.
Відносними протипоказаннями є: гострий і підгострий септичний ендокардит, прогресуючий розвиток дифузного гломерулонефриту, хронічна ниркова недостатність, хронічна і гостра печінкова недостатність, декомпенсація кровообігу, вади серця в стадії декомпенсації, міокардит і міокардіосклероз з порушенням загального кровообігу ІІ – ІІІ ступеня, гіпертонічна хвороба ІІІ стадії, виражений атеросклероз судин головного мозку, крововиливи в мозок, важкі розлади мозкового кровообігу, нефросклероз, тромбоемболічна хвороба, набряк легенів, загальний амілоїдоз, гостро перебігаючий і дисемінований туберкульоз, гострий ревматизм тощо.
З обережністю необхідно застосовувати трансфузії відмитих еритроцитів при тромбоемболічних станах.
Особливості до застосування: застосовувати лише в умовах стаціонару бажано в першій половині дня, після легкого сніданку або натще. Перед введенням довести температуру компоненту до кімнатної температури. Не підлягає застосування компонент з порушенням герметичності, маркування, при закінченні терміну придатності, при неправильному зберіганні , а також при зміну індивідуальних властивостій (кольору та інше.)
Перед трансфузією лікар повинен переконатися в ідентичності позначеної групи крові, резус–належності донора і реципієнта та провести візуальний контроль гемосередовища.
Під час переливання компоненту лікар, який виконує трансфузію, зобов’язаний, незалежно від проведених раніше обстежень і наявності записів, ОСОБИСТО провести такі контрольні дослідження:
– визначити групову належність крові реципієнта за системою АВ0 і звірити результат з даними медичної карти стаціонарного хворого;
– визначити групову належність еритроцитів донора і порівняти результат з даними на етикетці пластикатного контейнеру;
– провести проби на сумісність крові донора і реципієнта за системою АВ0 та резус–фактором – Rh0(D);
– провести пробу на сумісність між зразками компоненту крові у випадку гемотрансфузій від двох і більше донорів; провести біологічну пробу.
Компонент необхідно вводити за допомогою пристрою для переливання крові (ПК 22-02) з діаметром пор фільтра 170-120мкм, з дотримання правил асептики. Зважаючи на утворення мікроагрегатів під час зберігання , для введення компоненту бажано застосувати пристрій для переливання крові (ПК 23-01) з діаметром пор фільтра 20-40мкм. При трансфузії компоненту в обсязі, який перевищує 500мл, застосування пристрою з фільтром для видалення мікроагрегатів є обов’язковим.
Під час переливання необхідно проводити нагляд за реципієнтом. Швидке переливання холодного компоненту саме по собі може виявитися небезпечним.
Взаємодія з іншими препаратами: через ризик виникнення ушкодження еритроцитів не рекомендується додавати в дозу будь-які лікувальні препарати або розчини.
Умови зберігання: після виготовлення еритроцити відмиті повинні зберігатись в умовах холодильника від 2°С до б°С.
Термін придатності: 24 години.
Транспортування: транспортні засоби повинні бути обладнані холодильником з температурою від 2°С до 6°С, при відсутності холодильника обов’язково оснастити їх охолодженою ізотермічною ємністю. В процесі транспортування повинна бути забезпечена відсутність жорсткої вібрації контейнерів з відмитими еритроцитами.
Пакування: в полімерних контейнерах по (200±20) мл.
Виробник: Комунальний заклад охорони здоров’я Харківський обласний центр служби крові, Україна.
Адреса:61051, м. Харків, вул. Клочківська, 366, тел. (057) 337-85-01, факс: 337-83-38,
e-mail: medhospk@list.ru
Експедиція КЗОЗ ХОЦСК працює цілодобово: тел. 057(337-33-96), 057(337-84-95)
Нормативні посилання:
1. Наказ МОЗ України від 09.03.2010 №211 «Порядок контролю за дотриманням показників безпеки та якості донорської крові та її компонентів».
2. Наказ МОЗ України № 164 від 05.07.99 р.: «Інструкція з фракціонування донорської крові на її компоненти (плазма, еритроцити, тромбоцити, лейкоцити) та їх консервування», «Переливання компонентів та препаратів крові» (інструкція), «Контроль стерильності крові, її компонентів, препаратів, консервованого кісткового мозку, плазмозамінюючих та консервуючих розчинів, умов їх заготівлі».
3. Наказ МОЗ України № 385 від 01.08.05р. «Про інфекційну безпеку донорської крові та її компонентів».
